一、 引言:应用决定纯化策略——成本、规模与法规的权衡
酶纯化工艺的设计并非孤立的技术决策,其核心驱动力源于产品的最终应用。这本质上是一场在成本、生产规模与纯度/法规要求之间的战略权衡。一个酶制品的用途,无论是用于工业、诊断还是治疗,都从根本上决定了其纯化流程的复杂性、技术选型和最终的经济可行性。这一内在的制衡关系,我们可称之为“纯化三难困境”,它塑造了不同应用领域截然不同的工艺开发哲学。
例如,技术(工业)酶,如洗涤剂中使用的蛋白酶,其生产规模可达每年数吨,但对纯度的要求相对宽松,通常在25-90%之间。在此类应用中,首要目标是控制成本,因此工艺设计会有意规避昂贵的高分辨率层析技术。与此形成鲜明对比的是治疗性酶,其年产量通常仅为数公斤,但必须满足>99.9%的极高纯度标准,并遵循严苛的监管法规。这种巨大的差异揭示了一个根本性的经济现实:实现治疗级纯度所需的多步、高分辨率纯化流程,不仅本身成本高昂,而且每增加一个步骤都会导致产率的累积损失。这种特性使得以“吨”为单位的规模生产在经济上变得不切实际。此外,针对治疗性产品的严格法规要求,如病毒清除验证、宿主细胞蛋白(HCP)和DNA残留的严格控制,进一步增加了巨大的验证、文件和专用设备成本,而这些负担在工业酶的生产中几乎不存在。因此,不同的应用终点决定了从工程到商业运营的根本性差异。
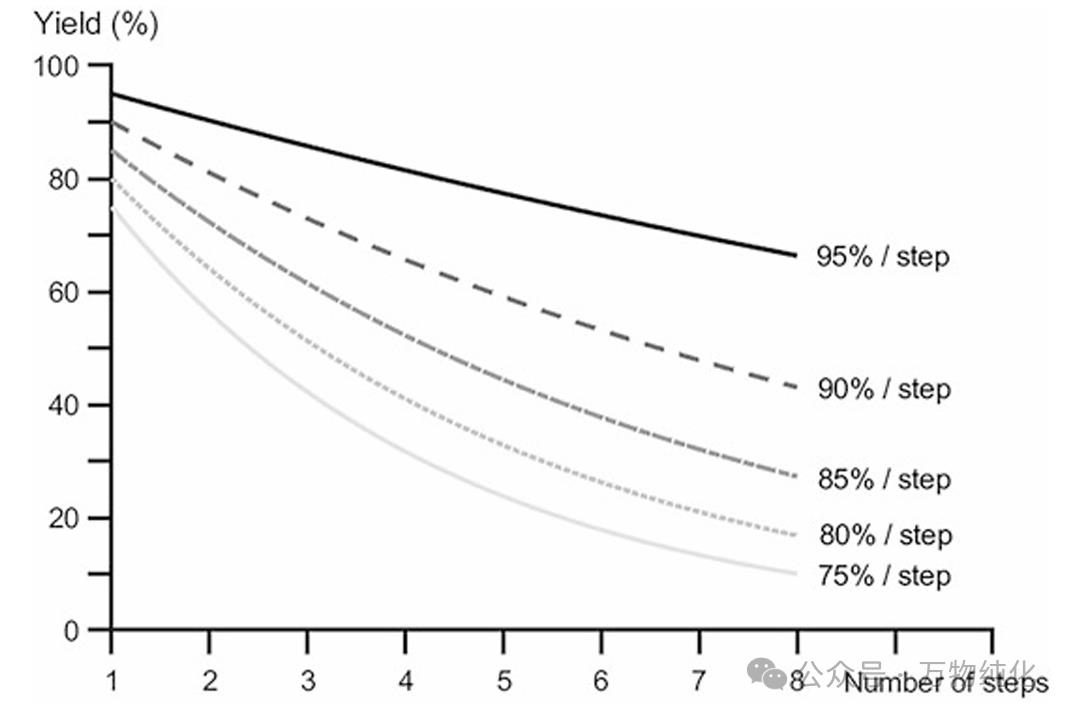
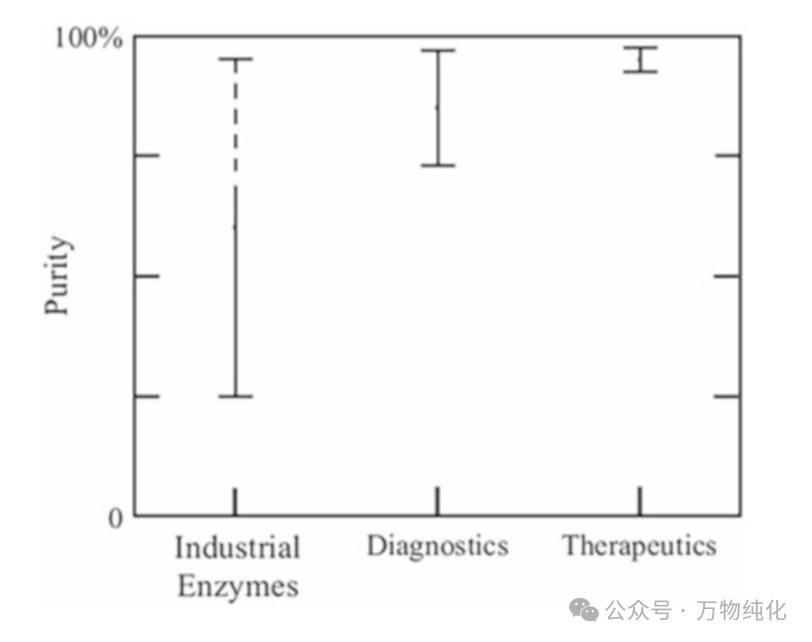
Fig. 10.2 不同产品所需的纯度
二、 核心评价指标:定义成功的下游工艺
为了系统地评估和优化任何酶纯化工艺,行业内普遍采用三个关键绩效指标(KPIs)。这些参数为工艺的成功与否提供了量化标准,并指导着工艺开发的每一个决策。
1. 纯度 (Purity, P): 纯度定义为目标产物量与总固体物质量(产物+杂质)之比。在实践中,酶的纯度通常通过比活性(单位/毫克总蛋白)来表征。随着纯化过程的推进,比活性会逐渐升高,并最终趋近于一个恒定的最大值。每一步纯化前后比活性的比值,即为纯化因子 (Purification Factor, PF),它量化了该步骤的纯化效果。
2. 产率 (Yield, Y): 产率是指目标酶回收的百分比。它分为单步产率 (Yi) 和贯穿整个流程的总产率 (Ytotal)。总产率是所有单步产率的乘积 (Ytotal = ∏Yi)。这一乘法关系凸显了工艺步骤数量对整体效率的决定性影响。即使每个步骤都有很高的产率(例如90%),一个多步流程的总产率也可能非常低。
3. 浓缩因子 (Concentration Factor, CF): 该指标衡量工艺对处理体积的缩减程度。对于工业生产而言,这是一个至关重要的参数,因为它直接关系到所需设备的大小、处理时间以及缓冲液和试剂的消耗量。工艺设计的普遍原则是在早期阶段就进行有效的体积缩减,并在后续流程中始终维持较高的产品浓度。
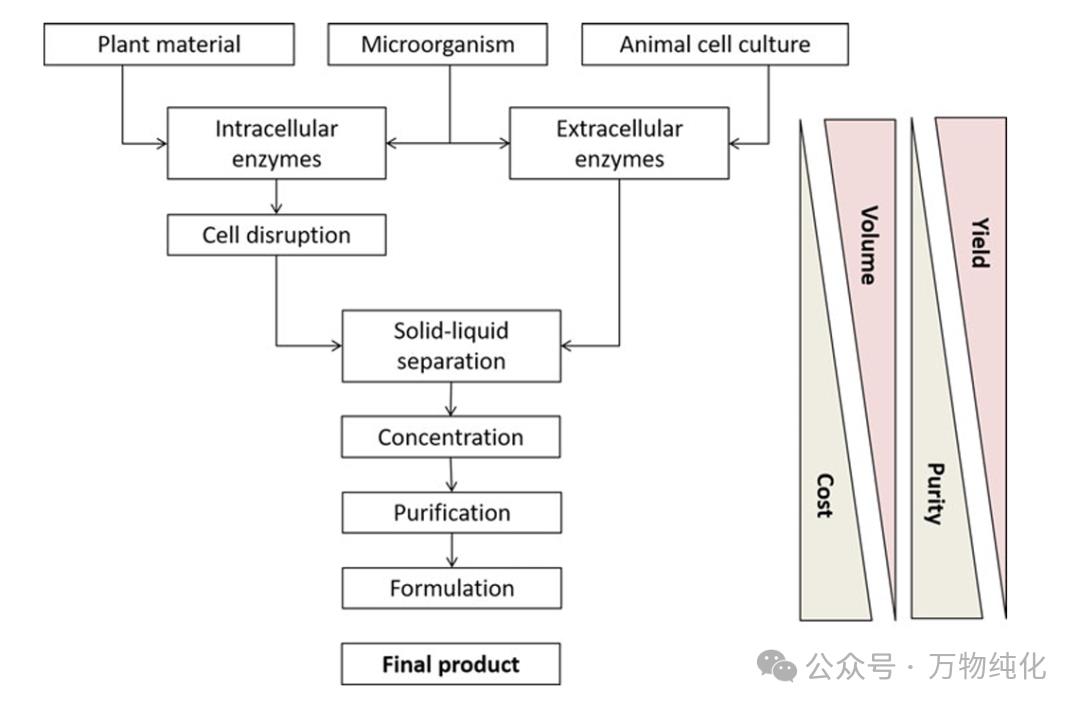
三、 酶纯化的应用光谱:三大领域的工艺对比
酶的应用领域决定了其纯化目标、工艺复杂度和纯度要求,形成了从工业级到治疗级的广阔光谱。以下是对三大主要应用领域的详细对比分析。
A. 技术(工业)酶
目标与理念: 核心目标是大批量、低成本地生产具有特定催化活性的酶制剂。高纯度通常并非必要条件,有时,共存的其他酶甚至对整体性能有益。例如,用于生物乙醇生产的酶制剂,其纯度要求通常不高。
工艺特点: 工艺流程相对简单。由于常使用GRAS(公认安全)认证的菌株(如芽孢杆菌、曲霉)进行分泌表达,初始回收步骤得以简化。通常仅包含固液分离(如离心、过滤)和一步浓缩(如沉淀、结晶),并主动避免使用高成本的高分辨率层析技术。
纯度要求: 25–90%。
B. 诊断用酶
目标与理念: 关键在于保证分析方法的高度特异性和灵敏度。纯化的首要任务是消除任何可能干扰检测结果的副反应活性。
工艺特点: 工艺复杂程度为中到高。必须采用层析、超滤等选择性强的技术。以葡萄糖氧化酶(GOD)为例,当用于血液样本检测时,其中的碳水化合物酶杂质影响不大;但若用于食品分析,这些杂质必须被彻底去除,以避免因样品中其他糖类分解而导致结果偏差。这表明,即使在同一类别内,具体的检测应用场景也会进一步细化纯化要求。
纯度要求: >95%。
C. 治疗性酶
目标与理念: 安全性与纯度是最高准则。工艺不仅要去除宿主细胞蛋白(HCP)和DNA,还必须清除潜在的病原体(如病毒)和与产品相关的杂质(如聚集体),以避免在患者体内引发免疫反应及其他副作用。
工艺特点: 极其复杂、多步骤且受到严格监管。流程中广泛采用高分辨率的先进技术,并且必须包含机制不同(正交)的关键步骤,如病毒清除,以确保产品的绝对安全。
纯度要求: >99.9%,并对特定污染物有严格的限量要求,例如DNA <10 ng/剂,HCP <100 ng/mg酶。
| 主要目标 | |||
| 纯度要求 | |||
| 年生产规模 | |||
| 工艺复杂度 | |||
| 关键技术 | |||
| 法规负担 |
四、 深度解析:治疗性酶下游工艺的“捕获-纯化-精纯”策略
尽管原始文献未明确使用此术语,但其描述的治疗性酶纯化流程完全符合生物制药行业公认的“捕获-纯化-精纯”(Capture-Purify-Polish, C-P-P)通用框架。理解这一框架,有助于我们从战略层面把握复杂多步工艺的内在逻辑。
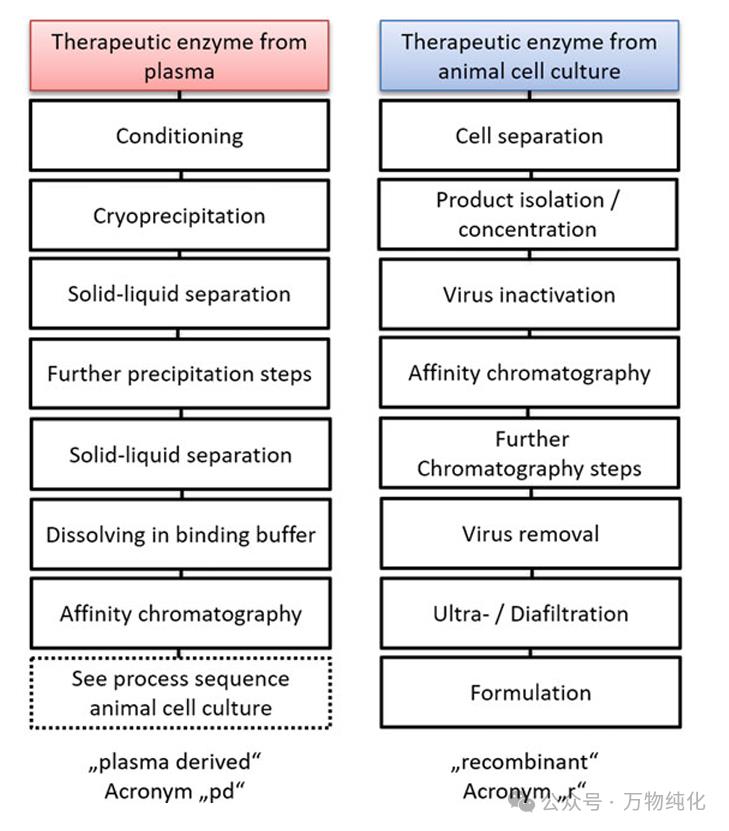
Fig. 10.4 来源于天然(血浆和组织)和动物细胞培养的治疗性酶的典型纯化流程
A. 捕获 (Capture): 从原料到浓缩粗品
目标: 从稀疏、复杂的起始料液中快速分离、浓缩和稳定目标产物,同时实现初步的体积缩减和杂质去除。
技术:
细胞分离:对于细胞培养生产的胞外酶,通常采用连续操作的碟式分离机或切向流微滤来去除细胞,澄清上清液。随后,通常会进行深层过滤和最终的0.2 μm除菌过滤,以保护下游的层析柱。
分步沉淀(科恩法,Cohn Process):对于血浆来源的产品,这是一种经典方法。通过精确控制乙醇浓度、pH和低温(如-3°C至-5°C),选择性地沉淀不同的血浆蛋白组分,从而在去除白蛋白等大量杂蛋白的同时,富集目标酶。这是一种高效的初始捕获和浓缩手段。
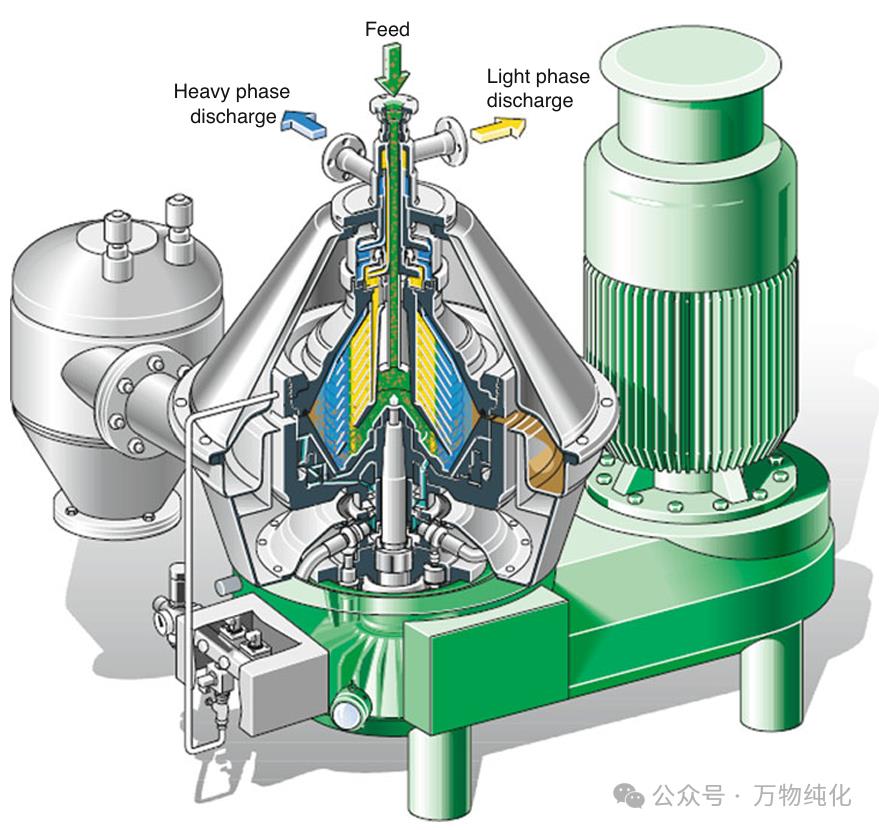
Fig. 10.5 带自动排渣功能的碟式分离机
B. 纯化 (Purify): 高分辨率层析法的核心应用
目标: 在此阶段实现纯度的最大飞跃,主要任务是去除与目标产物性质相近的宿主细胞蛋白等关键杂质。
技术:
离子交换层析 (IEX): 这是纯化工艺的“主力军”。凭借其高达100 g/L的载量,IEX既可用于捕获阶段的结合-洗脱模式以实现浓缩,也可用于纯化阶段的梯度洗脱模式以实现高分辨率分离。
亲和层析 (Affinity Chromatography): 这是纯化工具箱中最强大的技术,提供无与伦比的特异性。
组特异性配体: 可与一类具有共同特征的酶结合。例如,固定化金属离子亲和层析 (IMAC),利用Ni2+或Co2+等金属离子与组氨酸标签(His-tag)的结合,主要用于科研;Blue Sepharose,其配体Cibacron Blue 3G在结构上模拟辅因子NAD,可用于纯化脱氢酶和激酶等。
单特异性配体: 仅与特定的目标酶结合。对于高附加值的治疗性酶,开发这类配体(通常是单克隆抗体)在经济上是值得的。将单抗共价偶联到层析介质上,可实现从复杂的料液中一步捕获目标酶,极大提升纯化效率。

C. 精纯 (Polish): 安全、均一的最终保障
目标: 去除痕量杂质、与产品相关的变体(如聚集体),并确保产品的最终安全性和正确的制剂形式。
技术:
体积排阻层析 (SEC): 按分子大小进行分离。在精纯阶段,其主要作用是去除二聚体等多聚体,得到均一的单体活性产物。由于其载量较低,SEC通常只在纯化流程的末端,用于处理高度纯化和浓缩的料液。
病毒清除: 这是治疗性酶生产中一项至关重要的法规要求。其核心在于正交性清除原则,即工艺中必须包含至少两个基于不同物理原理的病毒清除步骤,以确保清除的稳健性。这是一个不可妥协的风险缓释策略。通过这两种正交方法的组合,病毒逃逸两个关卡的概率在统计学上变得微乎其微,从而确保产品的病毒安全性。
病毒过滤: 利用孔径极小的膜(如20 nm)进行机械筛分,物理截留病毒。
膜层析: 利用带正电荷的膜介质吸附表面带负电的病毒。这是一种基于电荷相互作用的深度过滤,而非表面截留。
制剂配方 (UF/DF 与冷冻干燥):
这是制备最终药品的最后步骤。通过超滤 (UF) 浓缩产品,再通过切向流过滤 (Diafiltration, DF) 进行缓冲液置换,将酶转移到稳定的储存缓冲液中。通常会加入聚山梨酯等稳定剂以防止聚集。最后,通过冷冻干燥将产品制成稳定的固体粉末,便于长期储存和运输。

五、 案例研究:重组因子VIIa的“定制化”纯化之路
重组凝血因子VIIa (rFVIIa) 的工业纯化过程,是理解“定制化”或“非平台化”治疗性酶工艺挑战的绝佳案例。与单克隆抗体(mAb)普遍采用Protein A亲和层析的“平台化”工艺不同,大多数治疗性酶缺乏这样的通用平台,其工艺开发需要从零开始,针对特定分子的特性进行量身定制。
rFVIIa的纯化流程可按C-P-P框架解析如下:
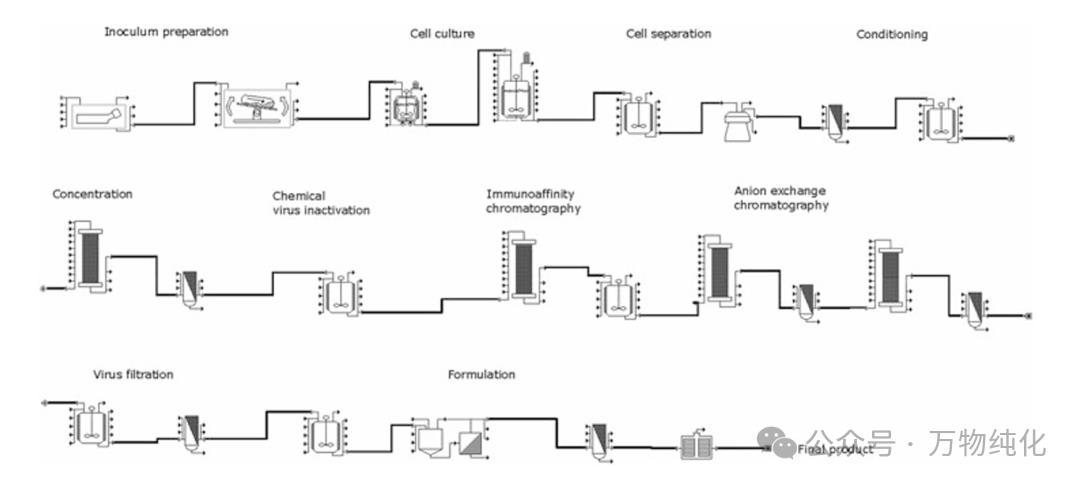
1. 捕获: 从表达人因子VII基因的BHK细胞培养液开始,通过碟式分离机和微滤进行细胞分离。澄清液经过调节后,进入第一步阴离子交换层析,实现初步浓缩和杂蛋白去除。
2. 纯化: 随后进行化学病毒灭活。核心纯化步骤是免疫亲和层析,使用针对FVII的特异性单克隆抗体作为配体,实现纯度的巨大提升。
3. 精纯: 此阶段包含两个非同寻常的步骤:两步连续的阴离子交换层析。从平台化工艺的角度看,重复使用相同机制的层析步骤是低效的。但在这个定制化流程中,它们有其特殊且必要的功能:去除从亲和柱上脱落的昂贵配体,并关键性地将前体酶FVII完全转化为活性形式FVIIa。之后,通过20 nm的病毒过滤完成正交病毒清除。最后,通过UF/DF、无菌过滤和冷冻干燥完成最终制剂。
rFVIIa的案例深刻揭示了非平台化分子工艺开发的复杂性。它表明,每一个新的治疗性酶都可能需要一个耗时且昂贵的从头开发过程,以解决其独特的纯化挑战。这也正是驱动该领域技术创新的核心动力,业界正不断探索如多模式层析、新型亲和配体等技术,以期为更多样的蛋白质药物提供更标准化、更高效的纯化解决方案。
六、 结论:下游工艺开发的金科玉律
综上所述,开发一个成功的酶纯化下游工艺,可遵循以下几条基本准则:
目标先行: 首先明确所需产品的纯度、活性和总量。
知己知彼: 充分表征目标酶和关键杂质的理化性质,以简化方法选择。
量化为王: 尽早建立能够检测目标分子、其活性以及关键污染物的可靠分析方法。
精简体积: 在工艺开始时就大幅减少体积,并在后续步骤中持续浓缩,以节省处理时间、设备尺寸和试剂消耗。
正交组合: 采用基于不同分离原理(如大小、电荷、疏水性、配体特异性)的方法组合,以达到更有效的纯化效果。
避免添加: 尽可能避免使用添加剂(如去污剂、蛋白酶抑制剂),因为它们后续必须被去除,且常给分析带来麻烦。
尽除内患: 在工艺早期就去除可能使目标酶变性的蛋白酶。
化繁为简: 尽可能减少纯化步骤,并合理组合,以优化总产率和工艺时间。
|
|
www.yc-e.com
|









